Histeroscopia
Histeroscopia vem do grego. Histero significa útero e scopeo, ver. A histeroscopia ou videohisteroscopia é, portanto, um exame de imagem do útero. Trata-se de um importante avanço tecnológico que permite à reprodução assistida descobrir e tratar causas de infertilidade feminina. O procedimento pode diagnosticar doenças intrauterinas, pólipos endometriais e endocervicais, mioma uterino submucoso, septo uterino, sinéquias, adenomiose e malformações. Diante dos seus resultados, é possível realizar a histeroscopia cirúrgica ou indicar técnicas de reprodução, como a Fertilização In Vitro (FIV).
Na histeroscopia, a via de acesso ao corpo feminino é o colo do útero, por isso, não são necessários cortes. O exame dura apenas 10 minutos aproximadamente, não precisa de repouso ou afastamento de atividades da paciente, depois de realizado. Também não há necessidade de anestesia. Pela baixa complexidade, pode ser feito em ambiente ambulatorial, no consultório do médico.
Indicações e contraindicações
A videohisteroscopia pode detectar causas de sangramento uterino anormal e estudar alterações no útero, relativas ao tamanho, forma ou outro aspecto que interfira na fertilidade. Mulheres com Dispositivo Intrauterino (DIU) sem fio também podem ser submetidas ao exame. Também é indicado para pesquisar abortos de repetição.
O exame não é obrigatório para as pacientes de Fertilização In Vitro, mas a histeroscopia faz-se necessária quando há indícios de anomalias no útero revelados por exames feitos previamente, como o ultrassom.
Mulheres grávidas, portadoras de doença inflamatória pélvica não tratada e sangramento volumoso não devem ser submetidas à histeroscopia.
O procedimento
A histeroscopia deve ser feita na primeira etapa do ciclo menstrual, entre o 5º e o 14º dia. Um pequeno tubo de até 4 mm de diâmetro é inserido no colo do útero, através da vagina. Na ponta dele há uma micro câmera e uma mini lanterninha.
Quando o tubo chega no útero, é inserido gás carbônico ou soro fisiológico por dentro dele para dilatar a cavidade uterina e facilitar a visualização das paredes do órgão pelo médico.
A anestesia só é necessária se aparecer alguma dificuldade no trajeto do tubo, sobretudo na passagem pelo colo do útero, uma vez que isso pode causar dor e desconforto na paciente.
Ao longo do exame, as imagens são transmitidas ao médico por meio de um monitor. Fotos também são tiradas para auxiliar no diagnóstico. Se houver alguma alteração, pode ser necessária a histeroscopia cirúrgica. Esta, em ambiente hospitalar e com anestesia.
Espermograma com capacitação ou recuperação espermática
O espermograma com capacitação espermática é o exame que revela a quantidade de espermatozoides móveis do homem, ou seja, aqueles capazes de realizar a fecundação. O seu resultado é fundamental para definir o método de reprodução assistida adequada. Mas, antes dele, é preciso conhecer o conceito do espermograma convencional.
O principal exame para checar a fertilidade dos homens é o espermograma. Num primeiro momento, ele avalia volume, pH e a liquefação do sêmen. Depois, são analisados os espermatozoides: quantidade, movimentação e forma.
Caso haja alguma irregularidade, o espermograma deve ter repetido. Se este novo exame der resultado conflitante com o primeiro, um terceiro deve ser programado. Os exames podem apontar problemas como oligozoospermia, astenozoospermia e teratozoospermia. São alterações referentes, respectivamente, à concentração, motilidade e morfologia dos espermatozoides. Caso alguma delas seja detectada pelo espermograma, o paciente deve ser encaminhado ao urologista para diagnóstico e tratamento.
O espermograma por capacitação espermática complementa o espermograma convencional. Ele checa a quantidade e a qualidade dos espermatozoides recuperados após o processamento seminal, que é a separação dos espermatozoides do líquido seminal. Essa divisão é feita porque o líquido seminal tem substâncias que podem causar reações indesejadas e contrações intensas no útero, o que dificulta a fecundação. Um exemplo dessas substâncias nocivas é a prostaglandina, lipídio ativo que age como hormônio. O processamento seminal é feito também para eliminar substâncias químicas e até mesmo bactérias do sêmen, evitando, assim, infecções.
O espermograma com capacitação espermática é feito em ambiente que simula o útero. É o resultado dele que orienta o médico a escolher a técnica de reprodução assistida mais adequada para o paciente, porque o exame revela a quantidade efetiva de espermatozoides capazes de fecundar o óvulo feminino, os chamados espermatozoides móveis.
Na técnica de swim-up, por exemplo, o espermograma de capacitação espermática é feito com o sêmen depositado no fundo de um tubo de ensaio e coberto pelo meio de cultura. Isso estimula os melhores espermatozoides a nadarem até a superfície. Após uma hora, esses que foram até o topo, os espermatozoides móveis, são selecionados.
Se o homem tiver menos de 5 milhões de espermatozoides móveis, ele pode conseguir engravidar a parceira com auxílio de algum tratamento de reprodução. Se ele tiver entre 1,5 e 2 milhões ou menos que isso, o mais indicado é a Fertilização In Vitro (FIV).
Para uma maior eficácia do exame, é recomendado que ele seja realizado em clínicas de medicina reprodutiva, como a Cenaferte, onde atende a Dra. Sofia Andrade. É a garantia de que a análise vai ser feita no ambiente com toda a estrutura técnica adequada e pelo profissional mais preparado o possível, o embriologista, pois treinado especificamente para análise seminal.
Punção testicular ou do epidídimo
Chama-se azoospermia a completa ausência de espermatozoides no sêmen após a ejaculação, que acomete até 2% dos homens, segundo estimativas. Ela pode ser obstrutiva ou não obstrutiva. Quando os gametas masculinos não são produzidos pelos testículos, é não obstrutiva. Se os espermatozoides forem fabricados, mas não aparecem no sêmen ejaculado por causa de barreiras nos ductos entre os testículos e a uretra, aí a azoospermia é considerada obstrutiva.
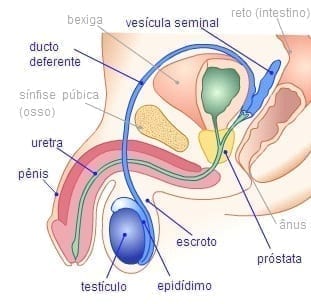
Esses casos acometem homens que realizaram vasectomia (cirurgia que interrompe a passagem dos espermatozoides dos testículos para o pênis), sofreram infecções ou traumatismos nos testículos. Que sofre de azoospermia obstrutiva precisa ter os espermatozoides retirados diretamente dos testículos ou do epidídimo que é um longo duto microscópico que leva os gametas masculinos em processo de maturação para o duto ou canal deferente. Este, por sua vez, leva até a vesícula seminal, uma espécie de armazém de espermatozoides já maduros, que produz um líquido viscoso que protege e nutre os gametas do homem.
A essa coleta artificial dos espermatozoides para utilização em algum tipo de tratamento de reprodução assistida é denominada punção testicular ou do epidídimo. Ela é realizada por meio de uma seringa bem fina e normalmente o paciente é sedado. Ele deve estar em jejum de 8 horas e o pós-operatório é feito à base de bolsas de gelo e analgésicos, quando necessário.
A depender do caso, as técnicas podem ser:
PESA (Percutaneous Epidydimal Sperm Aspiration) – Aspiração percutânea de espermatozoides do epidídimo. Técnica menos invasiva, pois o líquido seminal é retirado do epidídimo, é aplicada apenas anestesia local e não há necessidade de abrir o escroto. Procedimento indicado geralmente para quem fez vasectomia.
TESA (Testicular Sperm Aspiration) – Aspiração percutânea de espermatozoides do testículo. É a opção no caso dos espermatozoides não serem localizados vivos no epidídimo. Parecido com a PESA. A diferença é o local da retirada dos gametas, nos testículos, onde eles são fabricados.
TESE (Testicular Sperm Extraction) – Extração por biópsia dos espermatozoides do testículo. É uma pequena cirurgia, portanto, mais invasivo e complexo. Um corte de 2 centímetros é realizado no escroto para que o epidídimo seja exposto e o líquido seja extraído de seus túbulos.
MESA (Microsurgical Epidydimal Sperm Aspiration) – Aspiração microcirúrgica de espermatozoides do epidídimo.
Todas as técnicas permitem a coleta de gametas masculinos para fertilizar os óvulos via injeção intracitoplasmática de espermatozoide (ICSI). Ela consiste na introdução no óvulo de um único espermatozoide rigorosamente escolhido, para efetivar a fecundação.
As taxas de sucesso da punção testicular aliada à fertilização dependem, por exemplo, do número de embriões transferidos, idade da mulher e nível de excelência do local onde o procedimento é realizado. Mulheres com até 30 anos de idade chegam a ter 50% de efetividade da gravidez. Após os 42, esse índice gira em torno dos 15%.
Para esclarecer: não é certo que o material coletado tenha espermatozoides, independentemente da técnica adotada. Uma das poucas contraindicações da punção testicular é algum tipo de doença testicular grave, uma vez que o procedimento é relativamente simples e tranquilo.
Análise Embrionária Invasiva e Não Invasiva
A Análise Embrionária é o método pelo qual se estudam os cromossomos do embrião durante o tratamento da Fertilização in Vitro (FIV). Através dela, é possível descobrir se o bebê tem predisposição a apresentar malformações, como a síndrome de Down, por exemplo, entre outras.
A Análise Embrionária pode ser feita de duas formas: invasiva ou não invasiva. No primeiro caso, o mais tradicional, a biópsia (pequeno procedimento para obtenção de tecido) é realizada com a retirada de algumas células do embrião (estágio inicial do desenvolvimento do ser humano, após a fecundação do óvulo que, na fertilização in vitro, é feita em laboratório).
No segundo procedimento, mais moderno, o estudo é feito a partir da coleta de células no meio de cultivo, o líquido em que o embrião é conservado, antes da introdução no útero. Desta forma, o embrião é totalmente preservado.
Essa é a grande vantagem do Ge Screening Genético Não Invasivo (NICS) ou PGT-A não invasivo. Através dele, não há risco de danos ao embrião. Enquanto que, no procedimento tradicional, invasivo, o embrião pode ser lesionado no momento da retirada das células, inviabilizando assim a transferência daquele embrião.
A técnica identifica possíveis malformações que podem levar a complicações cerebrais, problemas cardíacos, microcefalia, defeitos congênitos em alguns órgãos, retardo no desenvolvimento ou até à morte nas primeiras horas após o nascimento. A presença de anomalias cromossômicas é uma das principais causas de interrupção natural da gravidez.
Quem deve fazer Análise Não Invasiva do Embrião?
Realizada no período de até cinco dias após a fecundação (inserção do espermatozoide no óvulo), a Análise Não Invasiva do Embrião é altamente recomendável para mulheres em idade avançada, a partir dos 38 a 40 anos. Por conta do processo de envelhecimento natural dos óvulos, há um risco maior do bebê apresentar malformações em gestações nesse período da vida feminina.
O homem consegue a cada 3 meses renovar todo o seu estoque de espermatozoides. No caso da mulher, é diferente. A mulher já nasce com todos os óvulos para o resto da vida. Quanto mais velha a mulher, portanto, mais velhos os óvulos. Por isso, o risco de danos ao DNA do óvulo é maior, devido a fatores como radicais livres, doenças como endometriose nos ovários, entre outros.
Além da idade, outros fatores a serem considerados para a Análise Não Invasiva do Embrião são o histórico familiar para mutação genética ou o fato da mulher já ter dado à luz a filhos com malformação. Por meio do exame genético, é possível identificar predisposição à anemia falciforme, por exemplo.
Avanços da Análise Não Invasiva do Embrião
A princípio, na Análise Não Invasiva do Embrião era relativamente comum a identificação de alterações cromossômicas em embriões normais. Isso ocorria, segundo pesquisadores, por causa de contaminações por células maternas que rodeiam o óvulo, chamadas de células da granulosa. Hoje, entretanto, com o desenvolvimento da técnica, esse risco é bem menor.
Isso porque, agora, são retiradas várias células do meio de cultivo (líquido no entorno do embrião, onde ele é conservado) representando assim células da massa celular interna (que gerará o bebê) e não apenas células do trofoectoderma (células que irão gerar apenas os tecidos extra-embrionários), como antigamente.
Caso seja identificada alguma malformação, o embrião não é selecionado para transferência ao útero e aquele embrião com o estudo cromossômico normal é então transferido.
Útero de substituição
Utilizado quando a paciente possui uma contraindicação médica para gestar ou não possui mais útero ou quando possui alterações na cavidade uterina que impossibilitem a implantação embrionária adequada.
Esta técnica é também utilizada em casais homoafetivos que desejam ser pais.
Para a utilização do útero de substituição, utiliza-se a fertilização invitro (FIV) para formação dos embriões (sendo os óvulos oriundos de estímulo ovariano na paciente que não irá gestar ou oriundos de ovodoação, ou seja, a paciente que abrigará o embrião apenas gestará sem ter vínculo genético com o embrião).
Após a formação do embrião por FIV, ele então é transferido para o útero de substituição. A paciente que irá doar temporariamente o útero precisa ser parente (até 4o grau) de um dos membros do casal e se for casada o esposo precisa consentir a gestação em documento assinado.
